১.৬ গ্যাস এর আংশিক চাপ ও ডাল্টন এর সূত্র
1.032g অক্সিজেন ও 0.573g CO2 এর মিশ্রণে CO2 এর মোল ভগ্নাংশ কত?
এর মোল =
এর মোল =
এর মোল ভগ্নাংশ =CO2 এর মোল÷মোট মোল(n1+n2)
Ai এর মাধ্যমে
১০ লক্ষ+ প্রশ্ন ডাটাবেজ
প্র্যাকটিস এর মাধ্যমে নিজেকে তৈরি করে ফেলো
উত্তর দিবে তোমার বই থেকে ও তোমার মত করে।
সারা দেশের শিক্ষার্থীদের মধ্যে নিজের অবস্থান যাচাই
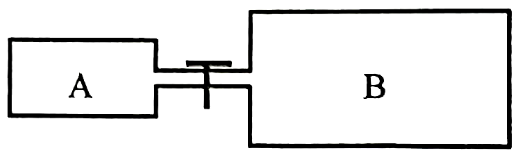 স্টপকর্ক বন্ধ অবস্থায়ঃ A গ্যাস= 102g, B গ্যাস= 28g
স্টপকর্ক বন্ধ অবস্থায়ঃ A গ্যাস= 102g, B গ্যাস= 28g
আণবিক ভরঃ A গ্যাস= 17, B গ্যাস= 2
স্টপকর্ক খোলা অবস্থায়ঃ মোট চাপ = 200mm(Hg)
স্টপকর্ক খোলা অবস্থায় A গ্যাসের আংশিক চাপ কত mm(Hg) ?
একটি আবদ্ধ পাত্রের মধ্যে A, B,C তিনটি গ্যাস মিশ্রিত অবস্থায় আছে এবং ওদের আংশিক চাপ যাথাক্রমে PA,PB ও PC। যদি B এর মোল সংখ্যা A এর দ্বিগুণ হয় এবং C এর মোল সংখ্যা B এর দ্বিগুণ হয় তবে...
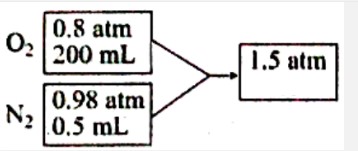
উপরিউক্ত পাত্রের মিশ্রনে N2 এর আংশিক চাপ কত?
STP তে একটি আয়তনের পাত্র মোল ভগ্নাংশের ভিত্তিতে 30% A, 60% B ও 10% C গ্যাসের মিশ্রণ ধারন করে এবং মিশ্রেণে A গ্যাসের পরিমাপ 14.28 g।