৪.১৯ বিক্রিয়া তাপ ও বন্ধন শক্তি
CH3Cl(I)+Cl2(g)→CH2Cl2+HCl(g), this reaction occurs with endothermic bond dissociation and exothermic bond formation . Here bond energy of C-H ,C-Cl,Cl-Cl and H-Cl are 430,328,243 and 433 kj/mol. What will be the value ∆H of above the reaction?
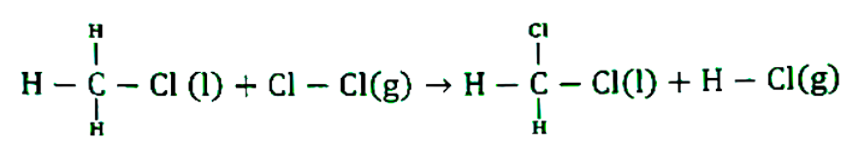 To calculate the enthalpy change (∆H) of the reaction, we need to use the bond dissociation energies of the bonds broken and formed during the reaction. The general equation to calculate the enthalpy change is:
To calculate the enthalpy change (∆H) of the reaction, we need to use the bond dissociation energies of the bonds broken and formed during the reaction. The general equation to calculate the enthalpy change is:
Given Bond Energies:
-
-
-
-
Reaction:
Identify the bonds broken
- 1 bond is broken.
- 1 bond is broken.
So, the total energy for bonds broken is:
Identify the bonds formed
- 1 bond is formed.
- 1 bond is formed.
So, the total energy for bonds formed is:
Calculate
Thus, the enthalpy change for the reaction is . This means the reaction is exothermic.
Ai এর মাধ্যমে
১০ লক্ষ+ প্রশ্ন ডাটাবেজ
প্র্যাকটিস এর মাধ্যমে নিজেকে তৈরি করে ফেলো
উত্তর দিবে তোমার বই থেকে ও তোমার মত করে।
সারা দেশের শিক্ষার্থীদের মধ্যে নিজের অবস্থান যাচাই
একটি বিক্রিয়ার তাপ রাসায়নিক সমীকরণ হলো:
(i) বিক্রিয়াটি কি তাপহারী না তাপোৎপাদী ?
(ii) স্থির চাপে বিক্রিয়ায় 4.4g উৎপন্ন হলে, এনথালপি পরিবর্তন কত হবে?
(i) নির্দিষ্ট তাপমাত্রায়, ভ্যান্ট হফ এর লেখচিত্র এর ক্ষেত্রে,
এর ক্ষেত্রে ঢাল ;
(ii) পটাশিয়াম সালফাইড এবং কপার (II) অক্সাইড উভয়ই আয়নিক যৌগ।
C-H, Cl-Cl , C-Cl ও H-Cl এর বন্ধনশক্তি যথাক্রমে 413, 242, 328, 433 kJ/mol হলে ,
+ 2HCl
এর বিক্রিয়া তাপ =?
বন্ধন বিয়োজন শক্তির মান সর্বাধিক কোনটি?